文章目录
- 要造出长长的多不饱和脂肪酸,需要很多氧气(无氧代谢会用不饱和脂肪酸来接收氢原子,由此产生饱和脂肪酸和反式脂肪酸)——合成DHA中的6个双键就需要6个氧原子,因此在出现氧气之前,地球上应该还没有DHA(至少极少)。 氧气出现后,海洋中的藻类(非植物)终于能用氧气来制造DHA了——这种“复杂的”脂类使得细胞能用来构建复杂的细胞结构,比如内质网、核膜、线粒体内的电子传递链,以及带有各种受体、转运蛋白、抗氧化酶的(流动性极佳的)细胞膜——细胞结构由此开始急剧复杂化。 细胞膜中嵌入的多不饱和脂肪酸,主要是AA、dGLA、EPA、DHA,它们一般位于甘油磷脂上的sn-2位置上。 复杂的结构(尤其是复杂的细胞膜)带来了复杂的功能,比如“信息处理”——DHA让动物们开始长出眼睛(视网膜的电活动需要DHA)和脑子——越来越“高级”的生命体开始涌现,头足动物、鱼类、两栖类、爬行类、鸟类和兽类陆续登场,而DHA一直都是它们的视网膜细胞、神经细胞内不可替代的油脂。 因此动物的眼和脑是DHA最集中的地方,尤其是脑内的灰质,更尤其是神经元之间形成连接的地方,最需要复杂的细胞膜结构的地方,也是生命体内的化学信号和电信号最集中的地方——突触。 灰质以多不饱和脂肪酸为主,其中DHA多于AA;而白质中则以单不饱和脂肪酸为主,AA多于DHA。 因此,当古人类终于来到海边采集“潮汐带”食物,从而能稳定、大量摄入DHA时,其脑内的灰质部分也急剧膨胀,直到自诩为“最高等生命”的智人出现。
- 漫长的演化史中,DHA的功能越来越复杂(背后是生命发展出了越来越多样的DHA受体);具体来说,这种古老的脂类能够: 影响生命的基础代谢率。通过对兽类(哺乳动物)和鸟类的脑、心、肾组织的研究,发现细胞膜中的DHA水平越高,其中的钠钾ATP酶(运输钠钾离子通过细胞膜,维持细胞内外的钠钾平衡,其能耗往往占整个生命体基础代谢率的1/5)的活性就越高(呈线性相关)——动物的脑是这种酶活性最高的地方,从而也是最需要(也最富含)DHA的地方。 钠钾ATP酶的能耗占整个脑部能耗的3/5!因为要不断发射电信号(靠改变钠钾离子的分布来实现)的神经元,极其依赖于及时维持的钠钾平衡。 影响细胞通讯。通过增强细胞膜上的G蛋白的可溶性,DHA能够影响G蛋白偶联受体的行为,从而间接影响各种细胞信号。比如,视网膜内的细胞膜上的视紫质就是一种G蛋白,DHA使其能够快速地接收光线(在此过程中DHA会与光受体分离,然后再被回收)。 消除体内炎症。DHA可以直接抑制NF-κB(细胞核转录因子κB)——这是免疫细胞(B细胞、T细胞)中的一种蛋白质,对氧化压力非常敏感——比如当活性氧簇水平升高时,或者其他炎症信号分子(比如主要由AA氧化成的类花生酸)出现时,它就会被激活,然后进入细胞核,上调许多促炎基因(比如白介素2、白介素6、白介素8、肿瘤坏死因子)的表达。而DHA可以直接抑制这个炎症的源头,从而降低全身的炎症水平。 DHA还可以间接抑制NF-κB。比如通过影响G蛋白偶联受体,减少磷脂酶A2的释放,从而减少类花生酸的合成;还有: 在局部炎症中,DHA(还有EPA)会从磷脂中被释放,转化成消炎的信号分子:消退素,它能下调NF-κB,从炎症部位驱除嗜中性粒细胞;和保护素(尤其是神经保护素),它主要出现在神经细胞、星形胶质细胞、循环组织和肺组织中,能促进神经再生,减少白细胞渗透,减少促炎和促进细胞凋亡的信号分子,从而保护神经细胞和视网膜细胞。 DHA还能上调细胞内的谷胱甘肽水平,进而降低细胞内的炎症水平。 促进神经发生。通过提升脑源性神经营养因子的水平,DHA能让脑内产生新的神经细胞和新的神经连接,并维持现有神经细胞的良好状态。 参与神经信号传递、形成记忆。当神经信号出现在突触时,此处的DHA(还有AA)会被(从磷脂中)释放进细胞液中,其中一部分转化成二级信号分子(类22碳酸——AA的话则是类花生酸),极少量被燃烧掉(β氧化),绝大部分则被磷脂迅速重新收纳——细胞膜借此过程得以重组,从而能强化神经通道,形成新的记忆。 改变基因表达、调节激素水平。DHA(还有EPA)会通过影响PPARγ、RXR、NF-κB来改变基因表达,从而增强生命体的整体适应能力、抗压能力;DHA水平还相关于瘦素水平和激素平衡。 将甲状腺素运输进脑。DHA参与合成甲状腺素转运蛋白,后者可以让甲状腺素穿过血脑屏障,从而让脑获得另一种对它至为紧要的营养素——碘。
- 生命体如此需要DHA,一般认为,是因为作为最不饱和的脂肪酸, DHA的6个双键可以让其分子呈微螺旋结构,从而能让细胞膜有最高的流动性。 但这似乎并非DHA最擅长的:DHA在低于零下44℃时就会凝固,相比来说,AA要到零下50℃才会凝固,EPA更要到零下54℃。 是的,DHA有着独特的分子形态:很长,很多双键。 不过DPA也是这样:同样有22个碳,只是比DHA少了一个双键(根据缺少的双键的位置,有ω-3和ω-6两种DPA);从化学角度看,这种差异本不会造成迥异的分子特性。 何况在陆地食物链中,DHA非常少,相比之下DPA却丰富多了——生命为何要去依赖一种稀有的,而不去(试图通过进化)开发利用另一种富庶的资源?毕竟只差了一个双键而已…… 我们看到,虽然在大型陆兽(比如大象)的身体组织内有大量的DPA;但是在其脑内,在其中的神经细胞膜内,却仍然谨守着可怜的那一丁点DHA……对DHA的“愚忠”大大限制了陆兽的相对脑容量(其脑容量相对于体型呈指数下降)。 为了理解这种愚忠,也许需要我们深入到量子生物学中(这是一个人类大体上还在摸黑的、全新的知识领域):比如6个双键的结构可能让π电子云出现极化,甚至能在双键之间传输,这使DHA能有奇特的、独一无二的电学特性;比如6个双键可能允许神经微管的伽马相干(γ coherence)…… 不过即使还不能完全理解DHA的不可替代性,我们只需要知道这点也就够了: 登上陆地后3亿多年的演化,也没能让陆地动物摆脱对DHA的依赖。 如果有意地将动物体内的DHA换成DPA,其组织功能就会明显恶化。
- 合成DHA似乎成了海藻们的绝技,陆地植物完全不解其中奥妙:后者擅长的是制造很短(18个碳)的多不饱和脂肪酸,尤以ω-6的LA为主,偶尔有少量的ALA。 淡水藻类由于会进行很多无氧代谢(产生饱和脂肪酸和反式脂肪酸),能制造的DHA也非常少。 是的,ALA与DHA一样都是光荣的ω-3,理论上是可以转化为后者的。于是对DHA不离不弃的陆生动物被迫接手了这个转化大业(主要在动物的营养中心——肝脏内进行)。 但这个转化的过程(ALA > EPA > DPA > DHA)漫长而繁琐,其中一些步骤的效率非常低,比如给ALA添加两个双键(“去饱和”),比如将EPA延长为DPA,但效率最低的还是给DPA再添加最后一个双键的过程——要完成这神奇一跃所需的“Δ6去饱和酶”非常少……所以转化往往都停滞在了DPA上——这就是陆兽们体内会有大量DPA的原因。 现代人饮食中大量的ω-6尤其是其中的LA,还会跟ALA竞争去饱和酶,更是大大拉低了ALA本就可怜的转化效率。 于是我们看到,虽然在陆兽的肝脏内有大量的ALA,少量的EPA,不少的DPA,但DHA却仍然稀有。 海豚与非洲水牛的肝脏中,ALA(18:3)、EPA(20:5)、DPA(22:5)、DHA(22:6)的比例。 对于成年人类来说,大量补充ALA虽然可以显著提高体内的EPA和DPA水平,但其(血液和母乳中的)DHA水平几乎纹丝不动。 母乳中的DHA水平对饮食中的DHA含量非常敏感。 即使在Δ6去饱和酶最为活跃的地方——人类婴儿的身体中,DHA的合成效率仍然不够理想:在饮食中只有ALA、缺少DHA的情况下,婴儿体内聚集DHA的速度仍然只有母乳喂养的婴儿的一半。 相比于只摄入ALA,让婴儿期的灵长类和人类直接摄入DHA能显著改善其视网膜功能。 随着年龄增长,人体内的Δ6去饱和酶的活性会急剧衰减。 转化速度慢,成功率低:植物的ω-3并不能给整个陆地食物链注满“灵油”。 于是我们看到,陆兽们的脑量完全无法跟上其体量的发展;相比之下,处在海洋食物链中的海兽就不受这种局限(比如斑马只有350g的脑,与其体重相当的海豚的脑则有1800g)。 DHA就这样成了大地上最为珍稀的油脂——只是一个双键,让DPA和陆兽们望洋兴叹。
- 人类的相对脑容量,却远远摆脱了这个禁锢。 陆兽的相对脑容量随着体型增大急剧下降——除了人类。 于是人类对DHA的需求量,也远远超出了陆地食物链的供给能力。不仅人类婴儿为了快速发育脑部,需要大量的DHA(好在最需要DHA的物种在最需要DHA的时候还有一定的自给自足能力);成年人为了维持脑的健康状态,也需要持续的DHA供应。 固然,人体能够非常有效地保存DHA,比如在视网膜和神经突触的电化学过程中不断被释放的DHA,绝大多数都会被迅速回收;细胞本身也有一定的维护机制,可以保护DHA少受氧化,并能恢复一些受损的DHA。(这个机制需要褪黑素,因此现代生活中的蓝光还会加速DHA的流失。) 但DHA毕竟还在不断损失着,即使很慢——据估计,脑内DHA的半衰期大约是2.5年。 再加上,在DHA短缺的情况下,人体还会从其他部位调拨DHA来优先保证脑的供应。于是脑很可能在很长一段时间内不会有缺乏DHA的迹象。 但是身体其他部位的情况就不容乐观了(我们在上面已经看到,DHA的工作远远不止限于脑内):缺乏DHA会导致基础代谢率下降、炎症水平上升、激素失衡、瘦素抵抗…… 当减肥困难、生理期紊乱、低密度脂蛋白水平过高时,都可以考虑是否有DHA摄入过少的可能…… 视网膜内的DHA匮乏,还会逐渐导致黄斑退化…… 当然,长期缺乏DHA最终还是会影响到脑部——星形胶质细胞受损,神经细胞不能正常工作……然后思维活力不足,记忆力下降,甚至脑萎缩…… 现代智人的平均脑容量,已经从10万年前的1490g下降到了1360g……DHA的普遍匮乏与之会否也有相关呢?(或许“现代人比原始人更聪明”,但也主要是因为“软件”而非“硬件”。) 关于DHA对各种神经退行性疾病的治疗作用,会有越来越多的相关研究。 我认为,为了让整个身体满状态运转,我们每天需要摄入至少2g的DHA。 这是我根据人类进化史做出的推测……是的,这个推荐量比可能在其他地方见到的(一般是几百毫克)要高多了。
- 为了补充DHA,我们不能依靠植物油里所谓的ω-3——ALA。 除了转化速度慢、成功率低(尤其是在成年人体内),ALA的氧化速度也非常快:提取出来后,每天甚至能氧化60%!所以那些所谓“富含ω-3”的植物油(比如亚麻籽油、夏威夷果油、核桃油),反而应该是我们躲之唯恐不及的…… 即使从完整的食物中摄取的ALA,在进入人体后也主要是被用来当燃料了,或者被合成为饱和脂肪酸、胆固醇。 在饮食中的DHA充足时,进入脑中的ALA(多不饱和脂肪酸可以轻易穿过血脑屏障)几乎有99%都会被燃烧(β氧化)掉。 ALA作为“必需脂肪酸”的地位正在被质疑,很可能:我们需要的只是其衍生物EPA和DHA,而完全不需要ALA本身。 为了补充DHA,我们需要直接摄入DHA。 植物不行,海藻怎样呢? 很可惜:作为地球上DHA的究极来源,海藻本身所含的DHA却非常少——一般在0.1mg/100g以下。这样即使每天只需补充500mg的DHA,摄入50公斤的海藻也还是不够。 那么从海藻中提取出来的DHA补剂呢?或者鱼油呢? 虽然DHA的氧化率比ALA要小多了,但每天也有5%左右——提取出来后,要经过多少天才能被我们吃下去呢?我们吃下去的,还能有多少完好的呢? 还是得吃食物本身:食物里的DHA不仅要稳定得多(由于各种抗氧化机制(维生素E、谷胱甘肽过氧化酶、碘)的存在),而且也好用得多——动物体内的DHA主要存在于甘油磷脂的sn-2位置上,这样最容易被身体吸收和利用。 应该吃什么动物呢? 虽然陆地动物能够合成一点DHA,但效率毕竟低下,那些无论肥瘦的畜肉禽肉,其中所含的DHA都几乎可以无视——再“草饲”也不行;只有其脑髓还算有可以看的DHA含量——只是要达到推荐摄入量,每天都要吃上400g左右……似乎并不是一个可以长期坚持的吃法。 淡水鱼里的“鲇形目”是一个例外,以后会说。 好在:海藻合成的DHA,最终都富集到了海洋动物们的脂肪内。最好的补充DHA的方法,就是吃各种海鲜:海贝、海鱼、海蟹、海虾……每100g的贻贝肉或牡蛎肉就含有250mg以上的DHA,更不用提秋刀鱼、三文鱼、带鱼、鲭鱼这些“油鱼”,每100g肉往往都有超过1g的DHA。 目前已知含DHA最多的应该是安康鱼肝——每100g含有3.6g。(鳕鱼肝油不算食物,也不推荐。) 所以:每周至少吃3斤油鱼(或再辅以其他海鲜),才好满足我们的整个身体,尤其是脑对这“灵油”的需求。 大约5~8亿年前,第一个脑诞生于大海中;数亿万年后,智慧终究还要回到故乡。
为记录下这个知识,怕以后找不到了,转载了此文,来源知乎:https://zhuanlan.zhihu.com/p/33275613
毫无悬念:在我们要系统了解对人脑来说什么营养素至为重要时,首先撞见的总是DHA。
DHA含有22个碳原子,其中有6个双键(与亚甲基交替出现)。

在生命体内,这是已知最长的脂肪酸之一(24碳的脂肪酸极为罕见),更是最不饱和的脂肪酸(没有之一)。
要造出长长的多不饱和脂肪酸,需要很多氧气(无氧代谢会用不饱和脂肪酸来接收氢原子,由此产生饱和脂肪酸和反式脂肪酸)——合成DHA中的6个双键就需要6个氧原子,因此在出现氧气之前,地球上应该还没有DHA(至少极少)。
氧气出现后,海洋中的藻类(非植物)终于能用氧气来制造DHA了——这种“复杂的”脂类使得细胞能用来构建复杂的细胞结构,比如内质网、核膜、线粒体内的电子传递链,以及带有各种受体、转运蛋白、抗氧化酶的(流动性极佳的)细胞膜——细胞结构由此开始急剧复杂化。
细胞膜中嵌入的多不饱和脂肪酸,主要是AA、dGLA、EPA、DHA,它们一般位于甘油磷脂上的sn-2位置上。
复杂的结构(尤其是复杂的细胞膜)带来了复杂的功能,比如“信息处理”——DHA让动物们开始长出眼睛(视网膜的电活动需要DHA)和脑子——越来越“高级”的生命体开始涌现,头足动物、鱼类、两栖类、爬行类、鸟类和兽类陆续登场,而DHA一直都是它们的视网膜细胞、神经细胞内不可替代的油脂。
因此动物的眼和脑是DHA最集中的地方,尤其是脑内的灰质,更尤其是神经元之间形成连接的地方,最需要复杂的细胞膜结构的地方,也是生命体内的化学信号和电信号最集中的地方——突触。
灰质以多不饱和脂肪酸为主,其中DHA多于AA;而白质中则以单不饱和脂肪酸为主,AA多于DHA。
因此,当古人类终于来到海边采集“潮汐带”食物,从而能稳定、大量摄入DHA时,其脑内的灰质部分也急剧膨胀,直到自诩为“最高等生命”的智人出现。
漫长的演化史中,DHA的功能越来越复杂(背后是生命发展出了越来越多样的DHA受体);具体来说,这种古老的脂类能够:
影响生命的基础代谢率。通过对兽类(哺乳动物)和鸟类的脑、心、肾组织的研究,发现细胞膜中的DHA水平越高,其中的钠钾ATP酶(运输钠钾离子通过细胞膜,维持细胞内外的钠钾平衡,其能耗往往占整个生命体基础代谢率的1/5)的活性就越高(呈线性相关)——动物的脑是这种酶活性最高的地方,从而也是最需要(也最富含)DHA的地方。
钠钾ATP酶的能耗占整个脑部能耗的3/5!因为要不断发射电信号(靠改变钠钾离子的分布来实现)的神经元,极其依赖于及时维持的钠钾平衡。
影响细胞通讯。通过增强细胞膜上的G蛋白的可溶性,DHA能够影响G蛋白偶联受体的行为,从而间接影响各种细胞信号。比如,视网膜内的细胞膜上的视紫质就是一种G蛋白,DHA使其能够快速地接收光线(在此过程中DHA会与光受体分离,然后再被回收)。
消除体内炎症。DHA可以直接抑制NF-κB(细胞核转录因子κB)——这是免疫细胞(B细胞、T细胞)中的一种蛋白质,对氧化压力非常敏感——比如当活性氧簇水平升高时,或者其他炎症信号分子(比如主要由AA氧化成的类花生酸)出现时,它就会被激活,然后进入细胞核,上调许多促炎基因(比如白介素2、白介素6、白介素8、肿瘤坏死因子)的表达。而DHA可以直接抑制这个炎症的源头,从而降低全身的炎症水平。
DHA还可以间接抑制NF-κB。比如通过影响G蛋白偶联受体,减少磷脂酶A2的释放,从而减少类花生酸的合成;还有:
在局部炎症中,DHA(还有EPA)会从磷脂中被释放,转化成消炎的信号分子:消退素,它能下调NF-κB,从炎症部位驱除嗜中性粒细胞;和保护素(尤其是神经保护素),它主要出现在神经细胞、星形胶质细胞、循环组织和肺组织中,能促进神经再生,减少白细胞渗透,减少促炎和促进细胞凋亡的信号分子,从而保护神经细胞和视网膜细胞。
DHA还能上调细胞内的谷胱甘肽水平,进而降低细胞内的炎症水平。
促进神经发生。通过提升脑源性神经营养因子的水平,DHA能让脑内产生新的神经细胞和新的神经连接,并维持现有神经细胞的良好状态。
参与神经信号传递、形成记忆。当神经信号出现在突触时,此处的DHA(还有AA)会被(从磷脂中)释放进细胞液中,其中一部分转化成二级信号分子(类22碳酸——AA的话则是类花生酸),极少量被燃烧掉(β氧化),绝大部分则被磷脂迅速重新收纳——细胞膜借此过程得以重组,从而能强化神经通道,形成新的记忆。
改变基因表达、调节激素水平。DHA(还有EPA)会通过影响PPARγ、RXR、NF-κB来改变基因表达,从而增强生命体的整体适应能力、抗压能力;DHA水平还相关于瘦素水平和激素平衡。
将甲状腺素运输进脑。DHA参与合成甲状腺素转运蛋白,后者可以让甲状腺素穿过血脑屏障,从而让脑获得另一种对它至为紧要的营养素——碘。
生命体如此需要DHA,一般认为,是因为作为最不饱和的脂肪酸, DHA的6个双键可以让其分子呈微螺旋结构,从而能让细胞膜有最高的流动性。
但这似乎并非DHA最擅长的:DHA在低于零下44℃时就会凝固,相比来说,AA要到零下50℃才会凝固,EPA更要到零下54℃。
是的,DHA有着独特的分子形态:很长,很多双键。
不过DPA也是这样:同样有22个碳,只是比DHA少了一个双键(根据缺少的双键的位置,有ω-3和ω-6两种DPA);从化学角度看,这种差异本不会造成迥异的分子特性。
何况在陆地食物链中,DHA非常少,相比之下DPA却丰富多了——生命为何要去依赖一种稀有的,而不去(试图通过进化)开发利用另一种富庶的资源?毕竟只差了一个双键而已……
我们看到,虽然在大型陆兽(比如大象)的身体组织内有大量的DPA;但是在其脑内,在其中的神经细胞膜内,却仍然谨守着可怜的那一丁点DHA……对DHA的“愚忠”大大限制了陆兽的相对脑容量(其脑容量相对于体型呈指数下降)。
为了理解这种愚忠,也许需要我们深入到量子生物学中(这是一个人类大体上还在摸黑的、全新的知识领域):比如6个双键的结构可能让π电子云出现极化,甚至能在双键之间传输,这使DHA能有奇特的、独一无二的电学特性;比如6个双键可能允许神经微管的伽马相干(γ coherence)……
不过即使还不能完全理解DHA的不可替代性,我们只需要知道这点也就够了:
登上陆地后3亿多年的演化,也没能让陆地动物摆脱对DHA的依赖。
如果有意地将动物体内的DHA换成DPA,其组织功能就会明显恶化。
合成DHA似乎成了海藻们的绝技,陆地植物完全不解其中奥妙:后者擅长的是制造很短(18个碳)的多不饱和脂肪酸,尤以ω-6的LA为主,偶尔有少量的ALA。
淡水藻类由于会进行很多无氧代谢(产生饱和脂肪酸和反式脂肪酸),能制造的DHA也非常少。
是的,ALA与DHA一样都是光荣的ω-3,理论上是可以转化为后者的。于是对DHA不离不弃的陆生动物被迫接手了这个转化大业(主要在动物的营养中心——肝脏内进行)。
但这个转化的过程(ALA > EPA > DPA > DHA)漫长而繁琐,其中一些步骤的效率非常低,比如给ALA添加两个双键(“去饱和”),比如将EPA延长为DPA,但效率最低的还是给DPA再添加最后一个双键的过程——要完成这神奇一跃所需的“Δ6去饱和酶”非常少……所以转化往往都停滞在了DPA上——这就是陆兽们体内会有大量DPA的原因。
现代人饮食中大量的ω-6尤其是其中的LA,还会跟ALA竞争去饱和酶,更是大大拉低了ALA本就可怜的转化效率。
于是我们看到,虽然在陆兽的肝脏内有大量的ALA,少量的EPA,不少的DPA,但DHA却仍然稀有。

海豚与非洲水牛的肝脏中,ALA(18:3)、EPA(20:5)、DPA(22:5)、DHA(22:6)的比例。
对于成年人类来说,大量补充ALA虽然可以显著提高体内的EPA和DPA水平,但其(血液和母乳中的)DHA水平几乎纹丝不动。
母乳中的DHA水平对饮食中的DHA含量非常敏感。
即使在Δ6去饱和酶最为活跃的地方——人类婴儿的身体中,DHA的合成效率仍然不够理想:在饮食中只有ALA、缺少DHA的情况下,婴儿体内聚集DHA的速度仍然只有母乳喂养的婴儿的一半。
相比于只摄入ALA,让婴儿期的灵长类和人类直接摄入DHA能显著改善其视网膜功能。
随着年龄增长,人体内的Δ6去饱和酶的活性会急剧衰减。
转化速度慢,成功率低:植物的ω-3并不能给整个陆地食物链注满“灵油”。
于是我们看到,陆兽们的脑量完全无法跟上其体量的发展;相比之下,处在海洋食物链中的海兽就不受这种局限(比如斑马只有350g的脑,与其体重相当的海豚的脑则有1800g)。
DHA就这样成了大地上最为珍稀的油脂——只是一个双键,让DPA和陆兽们望洋兴叹。
人类的相对脑容量,却远远摆脱了这个禁锢。
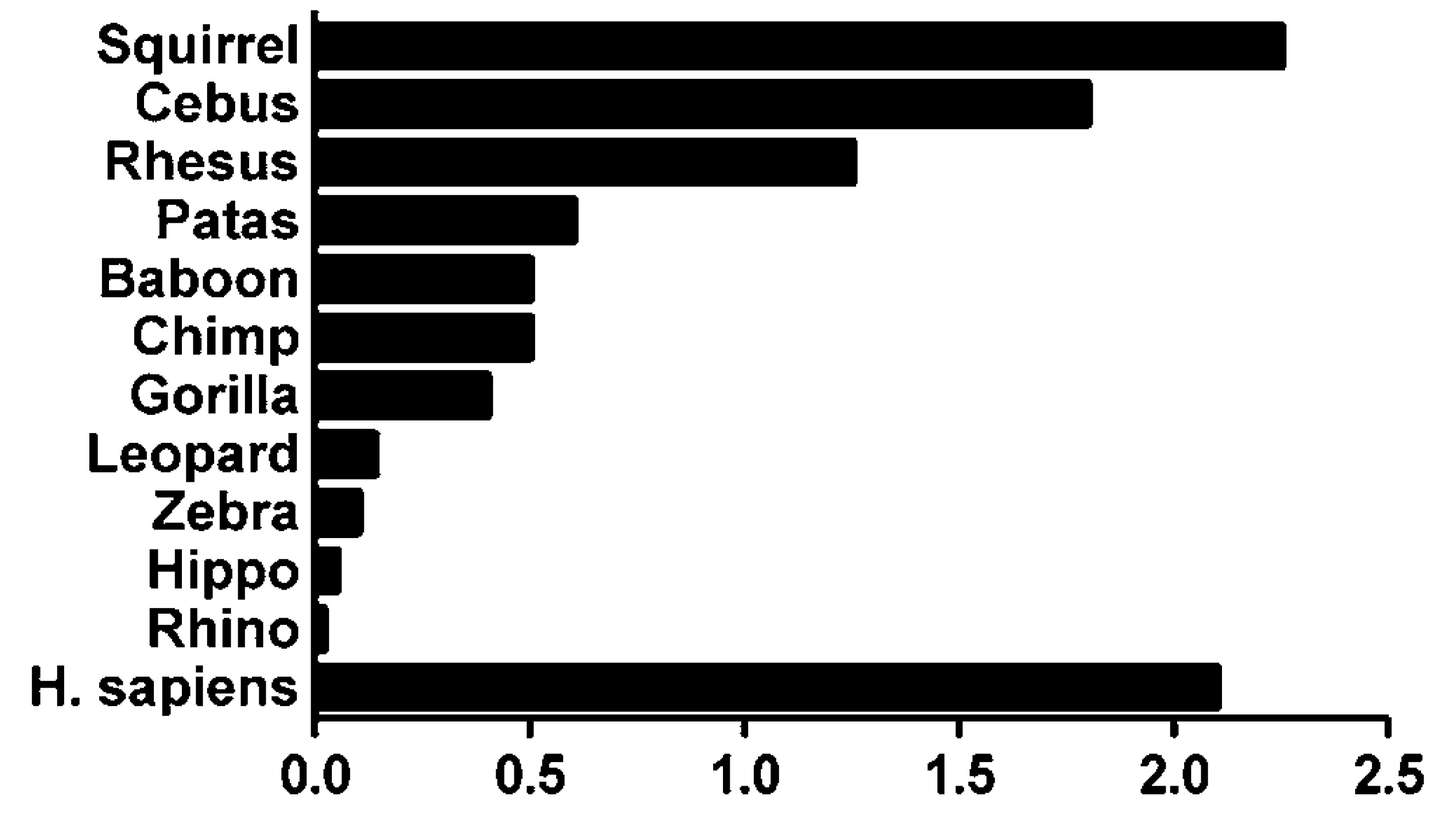
陆兽的相对脑容量随着体型增大急剧下降——除了人类。
于是人类对DHA的需求量,也远远超出了陆地食物链的供给能力。不仅人类婴儿为了快速发育脑部,需要大量的DHA(好在最需要DHA的物种在最需要DHA的时候还有一定的自给自足能力);成年人为了维持脑的健康状态,也需要持续的DHA供应。
固然,人体能够非常有效地保存DHA,比如在视网膜和神经突触的电化学过程中不断被释放的DHA,绝大多数都会被迅速回收;细胞本身也有一定的维护机制,可以保护DHA少受氧化,并能恢复一些受损的DHA。(这个机制需要褪黑素,因此现代生活中的蓝光还会加速DHA的流失。)
但DHA毕竟还在不断损失着,即使很慢——据估计,脑内DHA的半衰期大约是2.5年。
再加上,在DHA短缺的情况下,人体还会从其他部位调拨DHA来优先保证脑的供应。于是脑很可能在很长一段时间内不会有缺乏DHA的迹象。
但是身体其他部位的情况就不容乐观了(我们在上面已经看到,DHA的工作远远不止限于脑内):缺乏DHA会导致基础代谢率下降、炎症水平上升、激素失衡、瘦素抵抗……
当减肥困难、生理期紊乱、低密度脂蛋白水平过高时,都可以考虑是否有DHA摄入过少的可能……
视网膜内的DHA匮乏,还会逐渐导致黄斑退化……
当然,长期缺乏DHA最终还是会影响到脑部——星形胶质细胞受损,神经细胞不能正常工作……然后思维活力不足,记忆力下降,甚至脑萎缩……
现代智人的平均脑容量,已经从10万年前的1490g下降到了1360g……DHA的普遍匮乏与之会否也有相关呢?(或许“现代人比原始人更聪明”,但也主要是因为“软件”而非“硬件”。)
关于DHA对各种神经退行性疾病的治疗作用,会有越来越多的相关研究。
我认为,为了让整个身体满状态运转,我们每天需要摄入至少2g的DHA。
这是我根据人类进化史做出的推测……是的,这个推荐量比可能在其他地方见到的(一般是几百毫克)要高多了。
为了补充DHA,我们不能依靠植物油里所谓的ω-3——ALA。
除了转化速度慢、成功率低(尤其是在成年人体内),ALA的氧化速度也非常快:提取出来后,每天甚至能氧化60%!所以那些所谓“富含ω-3”的植物油(比如亚麻籽油、夏威夷果油、核桃油),反而应该是我们躲之唯恐不及的……
即使从完整的食物中摄取的ALA,在进入人体后也主要是被用来当燃料了,或者被合成为饱和脂肪酸、胆固醇。
在饮食中的DHA充足时,进入脑中的ALA(多不饱和脂肪酸可以轻易穿过血脑屏障)几乎有99%都会被燃烧(β氧化)掉。
ALA作为“必需脂肪酸”的地位正在被质疑,很可能:我们需要的只是其衍生物EPA和DHA,而完全不需要ALA本身。
为了补充DHA,我们需要直接摄入DHA。
植物不行,海藻怎样呢?
很可惜:作为地球上DHA的究极来源,海藻本身所含的DHA却非常少——一般在0.1mg/100g以下。这样即使每天只需补充500mg的DHA,摄入50公斤的海藻也还是不够。
那么从海藻中提取出来的DHA补剂呢?或者鱼油呢?
虽然DHA的氧化率比ALA要小多了,但每天也有5%左右——提取出来后,要经过多少天才能被我们吃下去呢?我们吃下去的,还能有多少完好的呢?
还是得吃食物本身:食物里的DHA不仅要稳定得多(由于各种抗氧化机制(维生素E、谷胱甘肽过氧化酶、碘)的存在),而且也好用得多——动物体内的DHA主要存在于甘油磷脂的sn-2位置上,这样最容易被身体吸收和利用。
应该吃什么动物呢?
虽然陆地动物能够合成一点DHA,但效率毕竟低下,那些无论肥瘦的畜肉禽肉,其中所含的DHA都几乎可以无视——再“草饲”也不行;只有其脑髓还算有可以看的DHA含量——只是要达到推荐摄入量,每天都要吃上400g左右……似乎并不是一个可以长期坚持的吃法。
淡水鱼里的“鲇形目”是一个例外,以后会说。
好在:海藻合成的DHA,最终都富集到了海洋动物们的脂肪内。最好的补充DHA的方法,就是吃各种海鲜:海贝、海鱼、海蟹、海虾……每100g的贻贝肉或牡蛎肉就含有250mg以上的DHA,更不用提秋刀鱼、三文鱼、带鱼、鲭鱼这些“油鱼”,每100g肉往往都有超过1g的DHA。
目前已知含DHA最多的应该是安康鱼肝——每100g含有3.6g。(鳕鱼肝油不算食物,也不推荐。)
所以:每周至少吃3斤油鱼(或再辅以其他海鲜),才好满足我们的整个身体,尤其是脑对这“灵油”的需求。
大约5~8亿年前,第一个脑诞生于大海中;数亿万年后,智慧终究还要回到故乡。
发表回复